海洋运输是货物运输的第一选择。世界各大海洋之中航行着超过50,000艘船只,承载了全世界几乎90%的货运总量。全球商船队的商业可行性在很大程度上取决于船只的外壳中国涂料在线coatingol.com。由植物和动物在船体水线以下的生长导致的生物淤积,尤其值得关注。海洋中的蛋白质、碳水化合物及其他微量营养素从船体与海水的最初接触阶段就开始粘附在船体上,由于这些营养物质会吸引海洋生物,这些海洋生物接着就停留在船体外壳上。在这个过程中形成的生物淤积层是一个非常复杂的栖息地—有几百种海洋生物相互作用、相互影响(正面或负面地),因此阻碍了船舶的移动能力(见图1)。

生物淤积使船体外壳表面明显变得粗糙,导致船舶行驶时的摩擦阻力剧烈增加。由此生成一种恶性循环:为了维持航行中的匀速,船舶就需要更多的能量和燃料,也就增加了与之相关的二氧化碳排放量。另外,船舶的可操作性也受到影响,受腐蚀的风险上升。由此,船舶需要更频繁地停留在码头进行清洗和维护。更短的维护周期和迅速上升的油料消耗,增加了海运公司的运输成本。
因此,对于保护船舶防止生物淤积的涂料一直有着非常高的需求。到目前为止,最有效地保护船体的方法是采用含有杀菌剂的防生物淤积的防污涂料。它们的作用机理是基于浸出作用,涂层中的活性毒性物质被不断地从涂层结构中溶解出来,进而迁移到船体外壳表面。在此,它们在船体外壳周围形成了一种杀菌环境,在微生物沉积在船体外壳之前,就能对其进行杀伤。过去,一直使用非常有效的杀菌剂如氢化三丁基锡(TBT),但调查研究发现,杀菌剂所释放的毒性不仅限于针对船体表面的微生物,它还会对海洋中的其他生物产生危害。这些生物面临这种环境下将会发生灭绝。基于这一调查结果,2008年,氢化三丁基锡(TBT)被禁止应用于全世界范围内的防污涂料中。今天可选择的活性剂是铜氧化物,与氢化三丁基锡相比,前者更具环境友好性,其作用机理也是浸出作用。但是,铜氧化物也是种重金属氧化物,溶解出的铜离子在高浓度时仍然具有毒性。因此,杀菌涂层正在被日益严格管控,需要找到一种高性能且无毒创新产品。
市场上大部分的无杀菌剂型沾污释放涂层提供了一种易清洁表面。其配方一般含有疏水性基料,像杂化有机硅树脂,有时掺入硅油或氟化物,这些物质会迁移到涂层表面。在静态环境下,例如,当船舶在装载或在半路停靠时,微生物会适应疏水环境并沉积在涂层表面,因为没有杀菌剂杀死它们。但是,由于涂层表面通常保持低表面能和高弹性状态,微生物与涂层间的附着强度比较弱,当船舶移动时,在动态环境下,剪切力足够强大,就可以分离生物沉积层并清洁船体外壳1。*另一方面,我们知道,亲水性的聚乙二醇(PEG),可以作为排斥剂防止微生物和细胞的粘附。这是因为它的水合强度及超高结构流动性2。当然,两种概念都显示了其对生物淤积应有的防污效果,近来的研究工作已经集中在将亲水基团和疏水基团的结合方面3。
我们的研究探索从SILIKOPON®EF化学结构开始,它是一款商用环氧有机硅杂化基料,以其防粘附性及机械强度和化学抗性而著称。这是一种疏水性树脂,通过亲水基团加以改性,得到一种两亲基料体系(见图2)。

这些聚合物可以利用由一个环氧开环反应及水解缩合反应组成的二元固化机理来得到光滑的表面。在这个固化过程中及在浸入水中之前,聚合物的亲水部分朝向漆膜表面,形成一道水合层,当将其形成完全涂层并涂布在船体上时,这层水合层就会遮盖在船舶外壳,使其如同就像水一样。水体生物不能将船舶的表面和周围的海水区分开来,这样一来就限制了它们在船体表面的沉积。在这里运用到了一种自然界的法则,即生命体总是寻求合适的栖息地才进行繁殖(见图3)。

在基料体系完成开发之后,很有必要对这种新建立的基料系统的沾污释放性能进行测试。与环境最相关的测试方法是海洋环境试验。然而这种实验需要做大量的准备工作,并不适合配方筛选实验,而且存在季节生长条件限制,特别是在北方海域的寒冷海水,这些差异性会阻碍连续性测试。要想得到快速且无关季节变化的独立实验结果,我们寻找到了新的评估生物淤积的方法。在与德国明斯特大学的合作中,开发了包含三个渐进步骤的方法,通过增加生物复杂性来模仿船上的海洋生物淤积。为此我们采用了微观研究和中观生态池研究与海水实地测试相结合的方法。
测试防污涂层的第一个步骤就是对由硅藻或单细胞细菌形成的生物膜层进行量化,例如通过用荧光染料4对核酸进行染色,或者通过分光光度法或者叶绿素荧光量化法5。尽管这个步骤与环境的相关性不那么大(因为自然的生态圈更加复杂),我们还是决定建立一个可以光合自养的共同培养的微观世界作为此次研究的第一步。对于确定培养的防污测试系统,我们选择可进行光合自养的硅藻-咖啡型双眉藻或三角褐指藻,同时选择异养型细菌-麦氏交替单胞菌。所有这三种细菌属于最先沉积在新鲜浸入海水表面的微生物品种。而咖啡型双眉藻更喜欢疏水性表面区域6,而三角褐指藻显然更喜欢沉积在亲水表面7-8。
为了减少微观实验和海水实地测试之间的差异,我们开发了一种中观生态池系统。我们设计了一个具有两个相邻水盆的亚克力玻璃水族箱。水盆中充满了海水并注射了从北部海域被生物层覆盖的石头上取下的生物质(见图4)。

我们选择的环境条件和营养素是可以进行光合自养的海藻和异养型细菌。水族箱的通气装置使涂装过的PVC板的水面有轻微波动,有利于以上微生物的生长,但没有对板表面施加剪切力。基于宏观实验的目视检查,每次在中观生态池的添加微生物,都带来相似的水相中的藻花及在PVC板未涂装区域生物淤积层的形成。安装好的PVC板在21摄氏度的条件下培养5周时间,每天照明16小时(静态生长环境)。此后,这些PVC板以每分钟60转的速度旋转运转一周(动态生长环境,最后将PVC板卸下并进行评估。旋转过程中,PVC板的外缘部分相对于板中心以2.45海里的速度进行运转。线速度随半径的减少和降低,因此,产生了一个对生物膜层施加的剪切力梯度。我们之所以选择这种相对较慢的旋转速度,就是找到那些在低剪切力下具有沾污释放性能的涂层。这种涂层很有可能在海水实地测试中展现出有效的沾污释放性能9。
最后,我们在德国胡克赛尔的北方海域进行了海水实地测试。这是一个具有寒冷海水和季节性生长特点的海洋实验场所。涂覆过防污涂料的PVC板在静态环境下从2017年3月开始暴露实验,直到2017年8月。PVC板每隔15天进行一次视觉检验,以监控生物淤积的等级。另外,板材的某一淤积区域使用硅胶刮刀以固定的方式刮掉以代替剪切力,来评估生物质对某个涂层的粘附情况如何。按照先前的实验结果,这种机械处理引起的污垢去除效果与水压200 bar下的喷水处理效果相当。
为了评估新开发的双亲基料的沾污释放性能,我们选择了具有不同亲水-疏水平衡值的从S1到S3的三种物料组分。新准备好的基料和DYNASYLAN® AMEO混合,加入2%的二羧酸二辛基锡作为催化剂,使用涂膜制备器和空气喷涂的方式在PVC片材和载玻片上涂布300微米的湿膜厚度,在室温下至少固化24小时,直至漆膜实干。本研究引入商用沾污释放涂料CI作为对比样(见表1)。

为了确保新开发涂料系统的沾污释放性能不是由毒性物质的浸出作用引起的,我们进行了条件培养基的毒性试验。为了测试条件培养基对细菌生理机能的影响,我们采用了一般海洋细菌麦氏交替单胞菌作为生物发光指示剂。研究了涂料的生长阻止性能和细胞溶解性能。结果显示,无论是S1到S3样品的涂层还是C1样品的涂层都没有任何的毒性(详见参考文献8)
接下来,不同基料在载玻片上的防污性能在麦氏交替单胞菌配合三角褐指藻或咖啡双眉藻的微观共培养条件下进行了测试,分别在光合自养生长环境下静态浸没2周。使用叶绿素荧光法量化生物膜层的生长。同时,我们建立了一套清洗流程,用以代替船舶快速行进过程中,水流产生的剪切力。载玻片的培养通过重复2次将同一片板浸入到新鲜的共培养液中来完成。重复实验需要考虑表面微生物的潜在变动,否则会影响的沾污释放性能的测试结果。叶绿素荧光法的量化被限制在涂层的中间区域,并统一为量化测试区域。接下来,我们将会列出标准化的藻类生物量以更方便对比。通过将每个涂层样品叶绿素荧光剂平均值和相应未涂装对比样的平均值通过比值计算反应标准化的藻类生物量程度。标准藻类生物量低于1显示涂层具有沾污释放性能(见图5)。
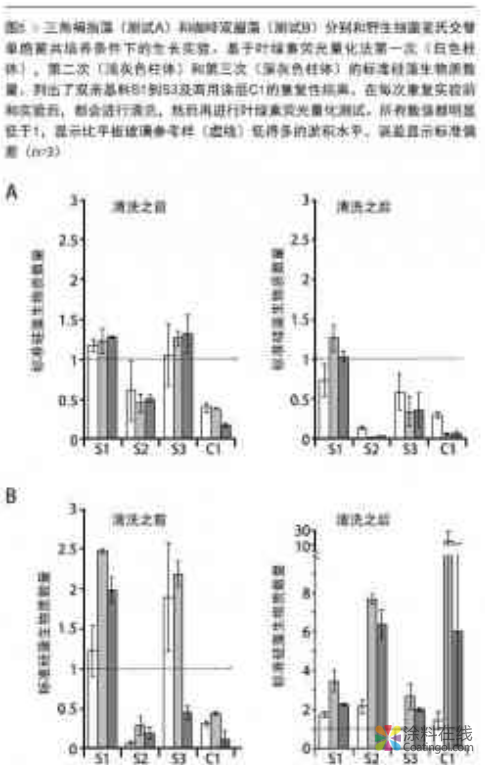
清洗前的结果仅证明生物体的粘附,清洗后的结果才能揭示这些生物品种的真正粘附性。如图所示,在清洗前,双亲基料S2相比于商用对比样C1,不管是在A共培养基还是在B共培养基都显示了较少的粘附数量。在清洗工序后,S2样和C1样在A共培养基仍然显示了良好的结果,却在B共培养基显示了较高的标准化荧光数值,表明了极少生物体品种对涂层的强粘附性。S1和S3在A共培养基和B共培养基都展示了较强的附着和粘附性。尽管从S1到S3,有一个亲水基团含量的线性增长,微观实验并没有出现直接对应关系。亲水性最高的S3基料和疏水变量最强的S1相比,在A培养基具有较低的粘附强度,尽管A共培养基含有三角褐指藻,更喜欢沉积在亲水性表面。看起来,亲水性的表面结构并不一定正比于亲水基含量。这些发现强调了在生物和化学系统间相互作用的复杂性,这对我们在没有生物性预先实验的情况下,很难预测出哪些样品会具有良好的沾污释放性能。
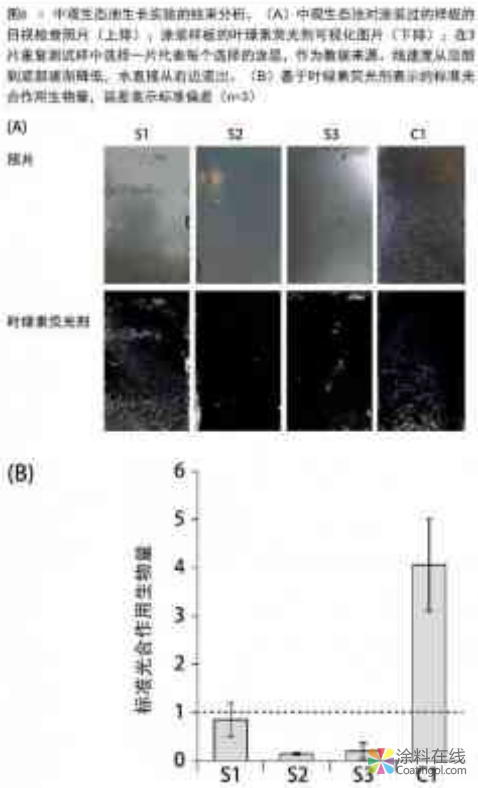
而对于中观生态池,涂装过的PVC板被浸入被人工引入藻花的自然海水中。实验用的海水和生物量取自于北部海域,以确保中观生态池可以尽可能低接近实际的海水实地测试。在将这些样品取下、评估前,基料S1到S3以及商用对比样C1在静态环境下暴露5周,然后在动态环境下暴露1周。在实验终点前,样品拆下不可能完全不损伤附着的生物膜层,也因此会影响实验结果。中观生态池终点时的目视检查显示双亲基料S2和S3几乎没有被沾污,而S1和C1则几乎被完全覆盖了一层生物膜(见图6,上部)。在所有涂层上可见的叶绿素荧光剂显示了和中观生态池目视检查结果非常相似的外观,表面生物膜层中含有可以进行光合作用的微生物(图6,下部和图表。)为了对生物质的光合作用进行量化,把叶绿素荧光剂在每一涂层的数量除以空白涂层的叶绿素荧光剂的数量,就可以计算出各自的标准光合生物量比值。数值低于1表示具有沾污释放的性能。在培养前,涂布的PVC板和未涂布的PVC板的叶绿素荧光剂是可以忽略的(未显示数据)。在中观生态池研究总结如下,每种涂层样品的沾污情况重复测试结果接近,表现为较低的标准偏差。这就表明沾污并不是偶然发生的,但显然它是有涂层表面的性能决定的。总之,S2样品是具有最佳表现的基料,远优于商用对比样C1。
海洋环境试验在德国胡克赛尔的北部海域进行,从2017年3月一直持续到2017年8月,在静态环境下,将PVC样板上的双亲基料S1-S3样品和商用对比样C1暴露在自然的有机生态圈中。静态的挂板实验不是很适合评估样品的沾污释放性能,因此,在目视检查时,引入了一道刮除流程,以此来模拟快速移动的船舶或喷水清洗。在暴露实验中,所有的涂层样品都产生了大量淤积。经过3个月的培养,除了S1样品,其余所有样品上附着的生物物质都可以刮除,在S1上仍然保留了一层薄生物质。经过5个月的培养,只有S2样品上的生物质可以被刮除。商用对比样C1的表面也发生了微生物的过度生长,有了很强粘附能量的生物质。总结起来,S2样品在实验中表现为最好的沾污释放涂料,其性能明显优于商用对比样C1(见图7)。
总而言之,开发的新型双亲环氧有机硅杂化基料可用于无杀菌剂的沾污释放涂料。在其作用模式中,这些基料的亲水基会在船舶外壳表面形成一道水化层,导致海洋生物的延迟识别作用。另一方面,这些基料的疏水部分则会赋予涂层表面一种易清洁效果,在动态环境下,得到良好的沾污释放性能。
新基料的测试采用多重研究的方法,从微观实验到中观生态池再到静态海洋环境试验。这种实验方法研究使我们可以独立于季节变化,有机会快速筛选基料的性能。虽然微观实验还是中观生态池,都不能代替真正的海洋环境试验, 但是,它们可以提供实际生态环境下沾污释放性能的大致趋势。
1、Beigbeder, A.; Degee, P.; Conlan, S.L.; Mutton, R.J.; Clare, A.S.; Pettitt, M.E.; Callow, M.E.; Callow, J.A.; Dubois, P. Biofouling 2008, 24, 291-302. Wynne, K.J.; Swain, G.W.; Fox, R.B.; Bullock, S.; Ulik, J. Biofouling 2000, 16, 277-288. Brady, R.F.; Singer, I.L. Biofouling 2000, 15, 73-81.
2、Prime, K.L.; Whitesides, G.M. J. Am. Chem. Soc. 1993, 115, 10714-10721. Ma, H.; Hyun, J.; Stiller, P.; Chilkoti, A. Adv. Mater. 2004, 16, 338-341. Schilp, S.; Kueller, A.; Rosenhahn, A.; Grunze, M.; Pettitt, M.E.; Callow, M.E.; Callow, J.A. Biointerphases 2007, 2, 143-150.
3、Galhenage, T.P.; Webster, D.C.; Moreira, A.M.S.; Burgett, R.J.; Staslien, S.J.; Vanderwal, L.; Finlay, J.A.; Franco, S.C.; Clare, A.S. J. Coat. Technol. Res. 2017, 14, 307-322. Hawkins, M.L.; Schott, S.S.; Grigoryan, B.; Rufin, M.A.; Ngo, B.K.D.; Vanderwal, L.; Stafslien, S.J.; Grunlan, M.A. Polym. Chem. 2017, 8, 5239-5251.
4、Vesterlund, S.; Paltta, J.; Karp, M.; Ouwehand, A.C. J. Microbiol.Methods 2005, 60, 225-233.
5、Galhenage, T.P.; Webster, D.C.; Moreira, A.M.S.; Burgett,R.J.; Staslien, S.J.; Vanderwal, L.; Finlay, J.A.; Franco, S.C.;Clare, A.S. J. Coat. Technol. Res. 2017, 14, 307-322. Sommer,S.; Ekin, A.; Webster, D.C.; Stafslien, S.J.; Daniels, J.;van der Wal, L.J.; Thompson, S.E.M.; Callow, M.E.; Callow,J.A. Biofouling 2010, 26, 961-972. Zhou, T.; Calabrese, D.R.;Taylor, W.; Finlay, J.A.; Callow, M.E.; Callow, J.A.; Fischer,D.; Kramer, E.J.; Ober, C.K. Biofouling 2014, 30, 589-604.
6、Cassè, F.; Swain, G.W. Int. Biodeterior. Biodegrad. 2006, 57,179-185. Zargiel, K.A.; Swain, G.W. Biofouling 2014, 30,115-129.
7、Buhmann, M.T.; Schulze, B.; Förderer, A.; Schleheck, D.;Kroth, P.G. J. Phycol. 2016, 52, 463-474. Dugdale, T.M.; Willis,A.; Wetherbee, R. Biophys. J. 2006, 90, L58-L60.
8、Zecher, K.; Aitha, V.P.; Heuer, K.; Ahlers, H.; Roland, K.; Fiedel,M.; Philipp, B. J. Microbiol. Methods 2018, 146, 10-114.